 Реферат: Исследование некоторых физико-химических свойств протеиназы Penicillium wortmannii
Реферат: Исследование некоторых физико-химических свойств протеиназы Penicillium wortmannii
Из анализа вышеприведённых данных можно сделать вывод, что для осаждения препарата протеиназы целесообразно применение этанола и изопропанола. В зависимости от назначения препарата возможно применение этого или иного растворителя с практически одинаковым эффектом.
3.2 Фракционирование протеолитического комплексного
препарата ферментов.
Полученный осаждением органическими растворителями препарат нами назван „протовортманин Г10х”. В дальнейшем представляло интерес изучить его компонентный состав и идентифицировать протеолитические фракции. Для этого был использован метод дискового электрофореза в ПААГ. Электорофорез вели с учётом „нейтральной’’природы протеолитического комплекса.
Компонентный состав препарата представлен четырьмя фракциями, отличающимися подвижностью в электрическом поле, размерами и интенсивностью окраски белковых полос.
Идентификацию протеолитических фракций проводили двумя способами: насыщением ПААГ денатурированным гемоглобином (pH 7,2) после дискового электрофореза и последующим выявлением прогидролизованных участков; экстракцией белкового спектра из ПААГ дистиллированной водой с определением протеолитической активности в экстрактах.
При гидролизе гемоглобина в ПААГ обнаружены две протеолитические фракции, которые проявились в виде двух светлых полос. Это свидетельствовало о том, что комплекс ферментов, гидролизующий белки в нейтральной области pH сложен и представлен двумя фракциями. Аналогичными были данные при использовании метода экстракции белковых полос из геля.
Таким образом, используя методы дискового электофореза было установлено, что компонентный состав полученного препарата представлен четырьмя фракциями, две из которых протеолитические. Кроме активного протеолитического комплекса препарат „протовортманин Г10х” содержал в своём составе глюкоамилазу (ГЛА 20ед/г) и альфаамилазу (3ед/г), сопутствующие ферменты, а также баластные вещества. Для получения гомогенных протеолитических фракций необходимо ввести более глубокую очистку.
3.3 Влияние температуры и рН на активность фермента.
Нами была поставлена цель определить рН и температурные оптимумы действия выделенных протеиназ Penicillium wortmannii 2091 и дать их сравнительную характеристику.
Нужное значение рН субстрата поддерживали с помощью 0,1М универсального буфера. Гидролиз вели при температуре 30оС в течение 30 минут. Ферментативную активность определяли стандартным методом [12].
Как видно на рис.2, препарат проявляет определённую активность в широкой зоне рН. Однако максимум активности наблюдается при различных значениях рН. Протеиназа 1 имеет оптимальное значение рН 7,2, в то время как протеиназа 2 – 10,0. Таким образом, протеиназа 1 имеет нейтральную природу, а протеиназа 2 – щелочную.
Температурный оптимум действия ферментов определяли в интервале температур 30 – 80оС при оптимальных значениях рН 7,2 и 10,0. На рис.3 показано влияние температуры на активность ферментов. Для протеиназы 1 максимальный гидролиз наблюдается при температуре 60оС, а протеиназы 2 – 40оС.
Таким образом, протеолитический комплекс Penicillium wortmannii 2091 представлен двумя ферментами, имеющими различные температурные и рН – оптимумы.
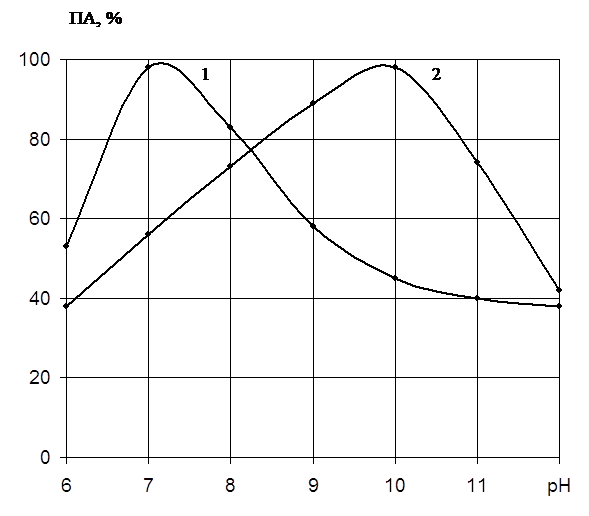 |
|||
|
|||
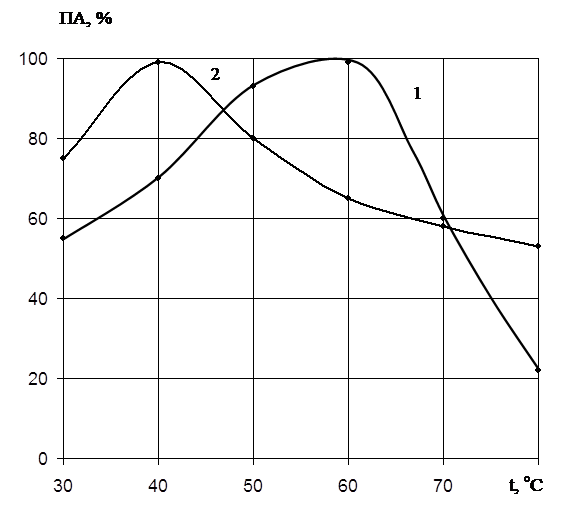 |
||||
|
||||
3.4 Определение молекулярной массы.
Молекулярную массу ферментов Penicillium wortmannii 2091 определяли методом гель-фильтрации на сефадексе У-100 [8].
Установлено, что соотношение объёма элюента, необходимого для выноса исследуемого белка из колонки (V – объём элюента) и объёма элюата, размещающемся в свободном (не занятом гранулами сефадекса) пространстве колонки (V0 – свободный объём), обратно пропорционально величине молекулярной массы белка. Для расчёта использовали формулу:
LgM=5,941-0,847 V/V0
Молекулярная масса протеиназы 1 оказалась равной 34500, протеиназы 2 – 20800, т.е. обе фракции относятся к низкомолекулярным белкам.
3.5 Исследование процессов кислотной и термической инактивации.
Изучение термо- и рН-стабильности ферментов часто несёт прикладной характер.
Исследование этих характеристик проводится остаточной активностью фермента после выдержки его раствора в течение некоторого времени при определённых рН и температуре [11].
Нами были проведены исследования кинетики кислотной и термической инактивации протеиназ Penicillium wortmannii 2091 и рассчитаны кинетические параметры этого процесса.
При изучении термо- и рН –стабильности раствор препарата выдерживали в фосфатном буфере в диапазоне рН от 5,0 до 12,0 и температур от 30 до 60оС. Периодически отбирали аликвотные доли раствора и определяли остаточную протеолитическую активность.
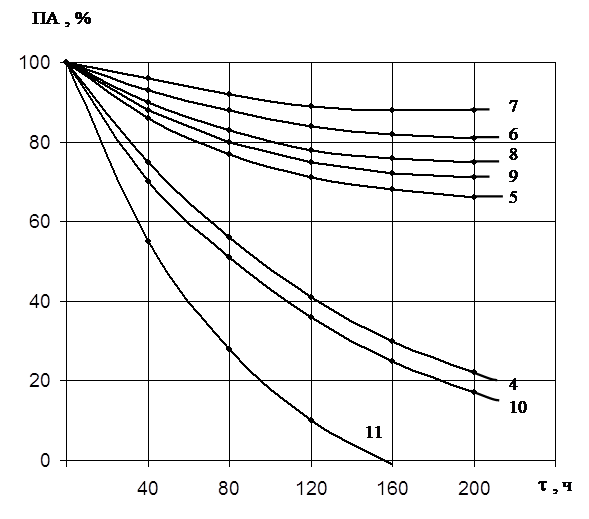
Полученные результаты по инактивации обоих ферментов показали, что протеиназа 1 сохраняет активность в широком диапазоне рН. При значении рН 7,0 через 200 часов фермент сохраняет около 90% активности (рис.4). При значениях рН 6,0 – 9,0 активность фермента снижается до 70 – 75%, это указывает на то, что фермент в указанном интервале не подвержен автолизу, а, следовательно, его нативная конформация обладает высокой стабильностью. При значениях рН ниже 6,0 и выше 11,0 каталитическая активность фермента быстро снижается.
Во всех случаях ПА/КлА-const, это свидетельствует о том, что мы имеем дело с одним ферментом.
Термическую инактивацию протеиназ изучали в интервале температур 30 – 60оС. Протеиназа 1 в области высокой рН-стабильности инактивируется почти полностью при температуре 60оС в течение 60 часов, в то время как протеиназа 2 при этой же температуре инактивируется полностью уже за 3 часа. Данные свидетельствуют о высокой термостабильности протеиназы 1. Инактивация протеиназы 2, происходящая при высокой температуре, по-видимому, определяется процессом разворачивания белковой глобулы.
Протеиназа 1, обладающая коллагенолитическим действием, нас интересует с практической точки зрения, поэтому были рассчитаны некоторые кинетические характеристики для этого фермента.
Если предположить, что в каждом элементарном акте процесса инактивации фермента под действием Н+ - ионов участвует одна его молекула, то кислотную инактивацию можно представить в виде реакции первого порядка. Кинетическое уравнение первого порядка имеет вид:
2,303 lg E0/E=K,
где Е0 – исходная активность фермента
Е – активность в момент времени
К – константа скорости инактивации, характеризующая потерю активности в течение часа, час-1.
 |
|||
|
|||
Остаточную активность выражали в процентах от исходной и затем использовали в расчётах констант инактивации. Величину находили, как среднее из 5 – 6 определений (табл.2).
Таблица 2.
Кислотная инактивация протеиназы 1 при температуре 500С.
| t, ч | Значения рН | |||||||
| 5,0 | 7,0 | 9,0 | 11,0 | |||||
| Е |
К*103ч-1 |
Е |
К*103ч-1 |
Е |
К*103ч-1 |
Е |
К*103ч-1 |
|
| 0 | 100 | 2 | 100 | 2 | 100 | 2 | 100 | 2 |
| 12 | 65,1 | 37,0 | 100 | 2 | 100 | 2 | 63,2 | 38,1 |
| 24 | 45,2 | 33,6 | 92,3 | 2,33 | 92,3 | 2,33 | 42,3 | 36,0 |
| 48 | 16,8 | 37,7 | 88,0 | 2,54 | 87,8 | 2,54 | 18,1 | 36,3 |
| 96 | 7,6 | 36,8 | 81,0 | 2,23 | 81,5 | 2,19 | 7,0 | 37,1 |
| 120 | 6,7 | 35,7 | 66,3 | 2,50 | 68,2 | 2,30 | 6,5 | 37,7 |
| 144 | 6,5 | 33,1 | 62,2 | 2,56 | 60,9 | 2,54 | 6,0 | 34,0 |
Как видно из табл.2, при определённом рН, значения констант достаточно близки друг к другу, максимальное отклонение от средних значений не превышает 10 – 15%, что вполне допустимо в исследованиях кинетики химических реакций. Это свидетельствует о том, что процесс инактивации протеиназы 1 является реакцией первого порядка. Различия в значениях при рН 5,0 и 11,0 и при рН 7,0 – 10,0 на целый порядок ещё раз указывают на лабильность фермента в слабо - кислой и слабо - щелочной зонах.
Страницы: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11


