 Реферат: Получение оксидов урана
Реферат: Получение оксидов урана
Некоторые соединения урана
Галогениды. Уран образует большое число соединений с галогенами:
UF3 UF4 UF5 UF6
UCl3 UCl4 UCl5 UCl6
UBr3 UBr4 UBr5
UI3 UI4
Стабильность галогенидов падает с возрастанием порядкового номера галогена и числа атомов галогена в соединении. Кроме того, известны оксигалогениды UO2Г2 и UOГ2.
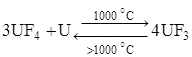 |
Трифторид UF3 может быть получен восстановлением тетрафторида водородом, алюминием или мелкодисперсным ураном при температуре около 1000 °С:
Трифторид изоморфен фторидам лантана и неодима. Он не растворяется в воде и разбавленных кислотах, медленно растворяется в концентрированных серной, азотной и хлорной кислотах, быстро – в смеси азотной и борной кислот, образуя UO22+. В соляной кислоте идет медленное растворение с образованием U3+.
Тетрафторид UF4 является исходным соединением для получения металлического урана. Хороший метод получения UF4 из перекиси урана осуществляется по схеме:
![]()
Холодные кислоты не растворяют
тетрафторид, при нагревании с концентрированными серной, ортофосфорной и
азотной кислотами он медленно растворяется.
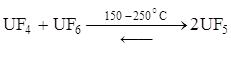 |
Пентафторид UF5 образуется при взаимодействии стехиометрических количеств тетра- и гексафторида урана:
Следовательно, пентафторид урана при нагревании диспропорционирует. Его можно получить также при действии фтористого водорода на пентахлорид урана или по реакции между тетрафторидом урана и фтором в необходимых пропорциях при 150–250 °С.
Гексафторид урана UF6 – легколетучее соединение, которое применяют для разделения изотопов урана в газовой фазе. Он не имеет жидкого состояния при атмосферном давлении и возгоняется при 56,5 °С. Давление его пара при комнатной температуре равно 120 мм рт. ст. Гексафторид урана получается действием фтора при температурах выше 220 °С на низшие фториды урана или фторирующих реагентов (AgF2, FeF3, BrF3, ClF3) на уран и его двуокись.
Органические вещества под действием гексафторида урана обугливаются. Устойчивы к нему только полностью фторированные органические соединения.
Тригалогениды UCl3, UBr3 и UI3 образуются при действии свободных галогенов или галогенводородов на уран, но одновременно получаются и тетрагалогениды.
Тригалогениды урана, свободные от тетрагалогенидов, можно получить действием галогенводородов на гидрид урана при нагревании:
Тригалогениды урана растворяются в воде и реагируют с ней с выделением водорода. В неполярных растворителях они нерастворимы.
Тетрагалогениды UCl4, UBr4 и UI4. Тетрахлорид и тетрабромид получают действием на двуокись урана при 500 °С соответственно четыреххлористого и четырехбромистого углерода или хлора в присутствии графита. Тетраиодид урана получается при действии паров иода на уран при давлении иода 100–200 мм рт. ст.
Все тетрагалогениды (кроме UF4) растворимы в воде, нерастворимы в неполярных растворителях.
Пентахлорид UCl5 получается действием хлора на тетрахлорид при 550 °С, а также четыреххлористого углерода на высшие оксиды урана при нагревании и под давлением:
Четыреххлористый углерод и сероуглерод растворяют пентахлорид урана. Спирты, эфиры, пиридин и ряд других органических соединений реагируют с пентахлоридом.
Гексахлорид UCl6. При нагревании пентахлорида в вакууме образуется гексахлорид, идет диспропорционирование и при этом гексафторид возгоняется:
Все галогениды урана, кроме фторидов, гигроскопичны, подвергаются гидролизу. Наименее гигроскопичны соединения урана (III), более гигроскопичны тетрагалогениды и еще более подвержены гидролизу гексагалогениды.
Оксигалогениды. При действии свободных галогенов или галогенводородов на оксиды урана при определенных условиях нагревания образуются оксигалогениды урана. Они могут быть также получены окислением тетрагалогенидов кислородом при 150 °С. Оксииодид крайне неустойчив. Оксигалогениды UVI хорошо растворимы в воде. Оксигалогениды UIV образуются при взаимодействии UO2 и тетрагалогенидов урана при высокой температуре, а также при гидролизе тетрагалогенидов урана. Оксигалогениды представляют собой растворимые в воде соединения.
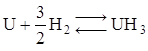 |
Гидрид UH3. Получается при действии паров воды на уран при 250°С или прямом взаимодействии элементов:
Положение равновесия зависит от температуры. Гидрид урана активен и служит исходным материалом для получения ряда соединений урана. Гидрид урана пирофорен. Растворами окислителей окисляется до иона UO22+. Гидрид урана растворим в соляной, азотной, горячей концентрированной серной, фосфорной и хлорной кислотах.
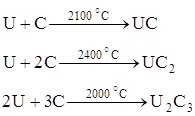 |
Карбиды. Уран образует три карбида стехиометрического состава UC, UC2 и U2C3. При непосредственном нагревании элементов в зависимости от взятых количеств образуются состава UC, UC2 или U2C3:
Карбид урана UC2 в измельченном состоянии пирофорен.
Комплексные соединения урана образуются с угольной, винной, лимонной, яблочной, молочной и другими органическими кислотами. В зависимости от концентрации адденда меняется соотношение комплексов различного состава. С ацетилацетонатом и другими дикетонами образуются растворимые в органических растворителях комплексы. Состав комплексных ионов может быть изображен формулой [U(CO3)n(OH)m]4-2m-n. В присутствии кислорода осуществляется переход в комплексный ион UVI.
В производстве широко применяется реакция комплексообразования уранил-иона с ортофосфорной кислотой:
где n = 1, 2, 3, 4, 5 и x = 0, 1, 2,…
Соли уранила образуют комплексные соединения с тиомочевиной. С теноилтрифторацетоном образуется комплекс UO2(TTA)2 . 2H2O. Получены также и другие комплексы урана.
II. ОКСИДЫ УРАНА. ИХ ХАРАКТЕРИСТИКА
Значение оксидов урана в его технологии
В результате аффинажа самыми различными способами уран получают в виде одного из таких соединений, как уранилнитрат, диуранат аммония, пероксид урана, уранилтрикарбонат аммония.
Операции превращения этих соединений в конечные продукты показаны на схеме:
![]() UO2(NO3)2 . 6H2O
Упарка
UO2(NO3)2 . 6H2O
Упарка
![]() (NH4)2U2O7
UO3
(NH4)2U2O7
UO3
![]()
![]()
![]() Прокаливание Восстановление UO2
Прокаливание Восстановление UO2
![]()
![]() UO4 . 2H2O
U3O8
UO4 . 2H2O
U3O8
(NH4)4[UO2(CO3)3]
![]()
![]()
![]() U Металлотермия Обработка HF
U Металлотермия Обработка HF
![]() UF4
UF4
![]() UF6 Фторирование
UF6 Фторирование
Следовательно, оксиды урана UO3, UO2 и U3O8 – важнейшие промежуточные продукты уранового производства при получении фторидов урана и металлического урана.
Кроме того, основой ТВЭЛов современных ядерных реакторов многих типов служит диоксид урана, который обладает высокой коррозионной и радиационной стойкостью. Применение огнеупорного UO2 дает возможность получать в реакторах значительно более высокие температуры, чем при использовании обычных металлических ТВЭЛов. Для изготовления таких ТВЭЛов используют, как правило, диоксид урана, обогащенный изотопом уран-235. Химические свойства такого диоксида аналогичны обычному. К диоксиду, обогащенному изотопом уран-235, предъявляются повышенные требования как по чистоте, так и по структуре и физическим свойствам [1].


