 Курсовая работа: Физические и фармакологические свойства основных сердечных гликозидов в зависимости от химического строения. Особенности заготовки сырья, содержащего сердечные гликозиды
Курсовая работа: Физические и фармакологические свойства основных сердечных гликозидов в зависимости от химического строения. Особенности заготовки сырья, содержащего сердечные гликозиды
К настоящему времени установлено строение 35 моносахаров сердечных гликозидов. Наиболее часто встречаются сахара (рис. 6 и 7):
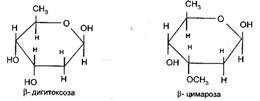
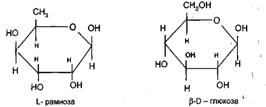
Рисунки 6 и 7. Сахара, входящие в состав сердечных гликозидов.
Длина сахарной цепочки влияет на растворимость сердечных гликозидов, кроме того сахара обуславливают способность кардиостероидов ингибировать АТФ-азы поверхностных мембран, а также влияют на фиксирование сердечных гликозидов в сердечной мышце. [3]
Содержание сердечных гликозидов в растениях, факторы, влияющие на их образование и накопление
Растений, содержащих сердечные гликозиды, немного, они составляют около 0,3% от общего числа видов флоры нашей страны. Наиболее богаты сердечными гликозидами растения следующих семейств: лилейных, лютиковых, норичниковых, капустных, кутровых, ластовневых. Кардиостероиды обнаружены также в секрете кожных желез жаб и в микроколичествах содержатся в бабочках.
Сердечные гликозиды содержатся в растворенном виде в клеточном соке различных органов растений: семенах (строфанты), листьях (наперстянка, ландыш), цветках (ландыш), подземных органах (кендырь коноплевый) и др. В растениях обычно содержится несколько близких по строению гликозидов, например из листьев наперстянки выделено около 70 гликозидов. Образованию и накоплению СГ в растениях способствуют свет, тепло. Содержание СГ в растениях, произрастающих на высоте (в горах, на возвышенностях), значительно выше. Большинство используемых в настоящее время лекарственных растений произрастает в тропиках (строфанты) или теплых климатических зонах (наперстянка, желтушник, горицвет и др.). Присутствие марганца и молибдена в почве увеличивает содержание сердечных гликозидов.
Обычно в растениях содержится 20-30 и более сердечных гликозидов и очень редко встречаются растения, содержащие один кардиостероид. Количественное содержание сердечных гликозидов находится в пределах 0,01-1%, составляя в среднем 0,2-0,5%. Особенно высоким содержанием кардиостероидов отличаются семена строфанта (до 3%) и желтушника (до 6%). [3]
Физико-химические свойства сердечных гликозидов
Сердечные гликозиды - кристаллические вещества бесцветные или беловатые, иногда с кремовым оттенком, не имеющие запаха и обладающие горьким вкусом.
Сердечные гликозиды не растворимы или трудно растворимы в воде, трудно растворимы в этиловом спирте. Растворимость в органических растворителях индивидуальна для каждого сердечного гликозида (например, строфантин в хлороформе не растворим, ланатозид С растворим мало, а эризимин -легко растворим). Кардиостероиды - оптически активные вещества, они характеризуются определенным углом вращения, имеют максимум поглощения при 215-220 нм (карденолиды) и 300 нм (буфадиенолиды). После обработки концентрированными кислотами у многих сердечных гликозидов появляется специфическая флуоресценция в УФ-свете. Например, ланатозиды, содержащиеся в наперстянке, после обработки смесью ледяной уксусной кислоты, концентрированной соляной кислоты и хлорамина имеют следующее свечение в УФ-свете: ла-натозид А \- желтое, ланатозид В - голубовато-зеленое, ланатозид С -голубое.
В зависимости от наличия полярных групп сердечные гликозиды условно делят на гидрофильные и гидрофобные. С увеличением числа полярных групп в молекуле (лактонное кольцо, альдегидная группа в положении 10, гидроксил в положении 5) гидрофильность соединения возрастает. К гидрофильным относят строфантин, конваллотоксин, к гидрофобным - дигитоксин, ацетилдигитоксин. От гидрофильности сердечных гликозидов зависят их фармакологические свойства: скорость и длительность действия, возможность образовывать комплексы с белками крови, проницаемость через липидные мембраны клетки и т.п. На полярность сердечных гликозидов оказывают влияние также характер сахарного фрагмента, его конформационные формы, относительное пространственное расположение агликона и углеводной части молекулы.
Химические свойства обусловлены:
1) наличием гликозидной связи (гидролиз ферментами и кислотами),
2) лактонного кольца (изомеризация под действием щелочей, образование окрашенных продуктов с ароматическими нитропроизводными в щелочной среде),
3) стероидной природой (образование окрашенных продуктов с кислотными реагентами: уксусный ангидрид, концентрированная серная кислота, трихлоруксусная кислота, треххлористая сурьма и др.).[6]
Кардиостероиды легко подвергаются кислотному и ферментативному гидролизу. Ферментативный гидролиз проходит под действием ферментов и характеризуется постепенным ступенчатым отщеплением сахаров. Гидролиз может протекать как под действием ферментов (гликозидаз, эстераз), содержащихся непосредственно в самом растении, - аутоферментация, так и с помощью различных ферментных препаратов: грибов (Aspergillus, Penicillium), панкреатического сока виноградной улитки, эмульсина из семян горького миндаля и др. В результате ферментативного гидролиза получают так называемые вторичные сердечные гликозиды. Ферментативный гидролиз широко используют для установления строения сердечных гликозидов и в производстве лекарственных препаратов.
При кислотном гидролизе используют кислоты слабой концен трации, чаще всего H2SO4(0,05 или 0,1 моль/л). В результате происходит отщепление всего углеводного фрагмента от стероидного ядра с последующим гидролизом до отдельных моносахаров.
Сахара, входящие в состав углеводных фрагментов сердечных гликозидов после гидролиза дают все цветные реакции, присущие углеводам (восстановление реактива Феллинга, аммиачного раствора серебра, образование окрашенных соединений с орцином, ксантгидролом, п-диметиламинобензальдегидом и т.д.).
Наибольшее распространение получила реакция с ксантгидролом, она используется в анализе и лекарственного растительного сырья (количественное определение ланатозида С в листьях наперстянки шерстистой) и препаратов сердечных гликозидов (целанид, дигоксин и др.) (рис. 8)
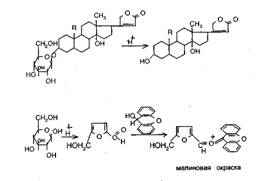
Рисунок 8. Реакция с ксантгидролом.
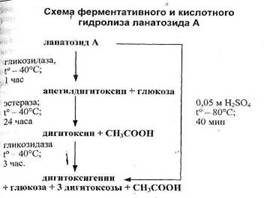
Реакция на 2,6-дезоксисахара (реакция Келлера-Килиани) с ледяной уксусной кислотой, концентрированной серной кислотой и следами Fe+ используется в качественном анализе субстанции и препарата «цимарин», «целанид», «дигитоксин». [3]
При взаимодействии сердечных гликозидов с реактивами, вызывающими дегидратацию гидроксильных групп стероидного ядра (особенно в 5 и 10 положениях) образуются ангидропроизводные различной окраски. Обычно эти реакции происходят в среде концентрированных кислот или под влиянием катализаторов (SbCl3, FnCl3 и др.). Кроме того, с концентрированными минеральными кислотами сердечные гликозиды могут образовывать окрашенные соединения (явление галохромии). Наибольшее распространение получили реакции с концентрированной серной кислотой. Так в качественном анализе конваллятоксина и строфантина используется реакция Либермана-Бурхарда (с уксусным ангидридом и конц. H2S04), в анализе строфантина-К еще и реакция с конц. H2S04.
В щелочной среде сердечные гликозиды образуют окрашенные соединения с нитропроизводными. Поскольку в образовании таких соединений основная роль принадлежит ненасыщенному лактонному кольцу, реакции, основанные на этом свойстве, часто объединяют в группу «реакции на лактонное кольцо». Наибольшее распространение в анализе препаратов сердечных гликозидов получи ли реакции: Раймонда (с 3% раствором м-динитробензола в бензоле), Легаля (с 5% раствором нитропруссида натрия), Татье (с 0,075% раствором 2,4-динитрофенилсульфона),' Балье (с 1% раствором пикрата натрия). Полученные в результате реакций комплексные соединения имеют оранжево-красную окраску, за исключением реакций Раймонда и Татье (соответственно окраска синяя и голубая). Наибольшее распространение получила реакция Легаля. Она используется в анализе практически всех субстанций и лекарственных форм. [10]
Заготовка сырья, содержащего сердечные гликозиды
При сборе, сушке и хранении сырья нужно создать условия, препятствующие ферментативному гидролизу гликозидов. Надземные части собирают в сухую погоду, в небольшую по объему тару (лучше корзины, ящики с отверстиями) и быстро, через 2-3 часа (чтобы не произошло самосогревание сырья) доставляют к месту сушки. Сушка для большинства видов рекомендуется быстрая, в тонком слое, при темп. 50-700. Можно при этой темп. выдержать сырье 1-2 часа, а затем, после дезактивации ферментов, досушивать его при обычной температуре.
Сроки заготовки сырья индивидуальны.
1) Листья наперстянки - Folia Digitalis (Наперстянка красная (пурпуровая) - Digitalis purpurea L.): сырье рекомендуется собирать в фазе цветения, в солнечный день, так как гликозиды накапливаются интенсивнее на свету. При возделывании наперстянки в виде однолетней культуры листья срезают 2-3 раза за лето без черешков (они затрудняют сушку, а биологически активных веществ не содержат).
2) Наперстянка шерстистая - Digitalis lanata Ehrh.: см. Наперстянка пурпурная. Для получения дигиланида С листья сушат при температуре 80°С, а дигоксина - не выше 45°С.
3) Цветки ландыша - Flores Convallariae
Листья ландыша - Folia Convallariae
Трава ландыша - Herba Convallariae
Ландыш майский - Convallaria majalis L. и его разновидности: ландыш кавказский - Convallaria L. transcaucasica Utk., ландыш дальневосточный (Кейске) - С. Keiskei: траву и листья ландыша срезают ножом или серпом на высоте 3-5 см от почвы, выше бурых чешуйчатых листьев, где расположены почки возобновления. Цветки срезают с остатком цветоноса не длиннее 20 см. Нельзя обрывать или выдергивать растения. Для быстрого восстановления зарослей срезают не более 25% от общего числа особей. Повторные заготовки в зависимости от района произрастания проводят через 3-6 лет. В южных районах заросли восстанавливаются быстрее. [2,6]


