 Курсовая работа: Энергоноситель
Курсовая работа: Энергоноситель
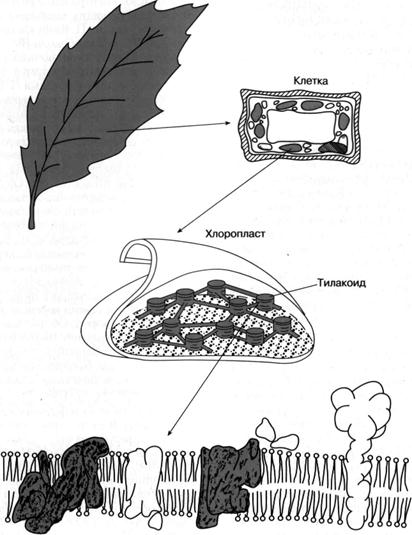
Мембрана тилакоида Рис. 4. Локализация фотосинтетического аппарата в клетке зеленого растения.
Пигмент-белковые комплексы можно разделить на две функциональные группы. Основная функция первой из них — "светособирающих" или "антенных" пигмент-белковых комплексов - состоит в эффективном улавливании энергии света. Более 90% всего хлорофилла сосредоточено именно в "антенных" комплексах. Большая их часть представляет собой белки с молекулярной массой от 20000 до 70000, на каждом из которых расположены 10 - 40 молекул хлорофилла. Помимо основного пигмента — хлорофилла а — в состав этих комплексов входит его аналог — хлорофилл б, а также каротиноиды — пигменты желтого или оранжевого цвета (один из них, бета-каротин, определяет окраску моркови). Цианобактерии содержат также бесхлорофилльные пигмент-белковые комплексы - фикобилины, окрашенные в синий или красный цвет. Они эффективно поглощают свет в области спектра, где хлорофилл имеет слабое поглощение, что позволяет осуществить более эффективное улавливание солнечной энергии.
Энергия возбуждения от светособирающих пигментов с очень высокой эффективностью (близкой к 100%) передается на хлорофилл другой группы пигмент-белковых комплексов - фотохимические реакционные центры. Их основная и важнейшая для всей биосферы функция состоит в том, чтобы преобразовать энергию электронного возбуждения хлорофилла (полученную в результате поглощения света в данном комплексе или в результате миграции возбуждения от светособирающих комплексов) в энергию разделенных зарядов, подобно тому, как это происходит в реакции Красновского, описанной выше.
У кислородвыделяющих организмов имеется два типа реакционных центров, функционирующих в так называемых фотосистеме 1 (ФС-1) и фотосистеме 2 (ФС-2) (рис. 5). Аналоги каждого из этих реакционных центров обнаружены у ряда фотосинте-зируюших бактерий, и молекулярная структура одного из них, выделенного из пурпурной бактерии Rhodopseudomonas viridis, впервые была установлена с помощью рентгеноструктурного анализа. Необходимо отметить, что значительная часть знаний о структурной и функциональной организации фотосинтетических реакционных центров получена при помощи изучения именно бактериальных реакционных центров. Они отличаются высокой стабильностью в изолированном из мембраны состоянии, и именно из них удалось впервые получить
кристаллы, использование которых в рентгено-структурных исследованиях позволило получить данные о молекулярной структуре реакционного центра. За эту работу группа немецких исследователей в 1988 году получила Нобелевскую премию.
Бактериальный реакционный центр состоит из трех полипептидов с молекулярной массой от 24000 до 32000, на которых расположены молекулы одного из представителей хлорофиллов - бактериохлорофилла (Бхл) и две молекулы его безмагниевого производного — бактериофеофитина (Бфф). Две из четырех молекул Бхл расположены настолько близко друг к другу (около 3 Å), что формируют компактное образование — димер (П), а четыре другие одиночные молекулы пигментов образуют две симметричные по отношению к П цепочки Бхл—Бфф. Энергия электронного возбуждения, полученная в результате поглощения света пигментами самого реакционного центра или в результате ее миграции от светособирающих комплексов, локализуется в конечном счете на П. Возбужденный П, обозначаемый как П*, за время около 10-12 сек передает свой электрон на одну из одиночных молекул пигмента, так что в результате образуется первичное состояние с разделенными зарядами П+Бфф-. Это состояние обладает очень коротким временем жизни (около 10~8 сек) вследствие возможного возврата электрона от Бфео- к П+. Однако вероятность этого процесса очень низка благодаря более быстрому (2 • 10-10 сек) "прямому" переносу от Бфео- к "стабильному" акцептору электрона, получившему название Q. При этом образуется состояние П+БфеоQ-, время жизни которого уже составляет около 10-3 сек. Необходимо отметить очень высокую эффективность описанных стадий фоторазделения зарядов. Так, квантовая эффективность, то есть доля поглощенных квантов, вызвавших перенос электрона, близка к 100%. Энергетическая эффективность, то есть доля энергии возбуждения, запасенной в результате фотохимического акта, составляет свыше 90% для первой стадии переноса электрона и около 50 - 70% для второй. Об изумительном совершенстве этой уникальной биологической "машины" свидетельствует, например, тот факт, что с такой же эффективностью фотоперенос электрона в реакционном центре осуществляется даже при температуре жидкого гелия (-271°С).
Основным итогом фотохимической стадии преобразования энергии света у кислородвыделяющих фотосинтезируюших организмов является фотоперенос электронов от воды к НАДФ+. Обе фотосистемы (ФС-1 и ФС-2) участвуют в этом процессе, обеспечивая двухступенчатое поступление энергии для его протекания. ФС-2 осуществляет окисление воды с образованием молекулярного кислорода, согласно реакции: 2Н20 + 4hv —О2 + 4е+ 4Н+, где hv обозначает квант света, е—электрон. В результате фотохимического акта реакционного центра ФС-2 образуется самый сильный биологический окислитель — окисленный хлорофилл, который окисляет воду с участием марганецсодержащей энзиматической системы. Электроны, оторванные от воды, через цепь темновых реакций поступают на ФС-1, использующую их для фотовосстановления НАДФ+ до НАДФН, которое тоже осуществляется с участием специальной энзиматической системы. Окисление воды, а также перенос электронов от ФС-2 к ФС-1 приводит к появлению разности концент-
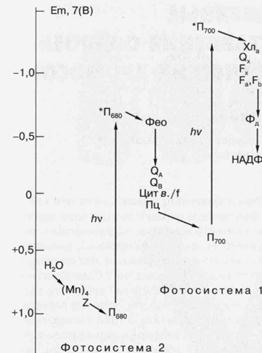
Рис. 5. Схематическое изображение фотосинтетической цепи переноса электрона в хлоропласах растений и цианобактерий. (Мп)4 - Комплекс из четырех атомов Мп, связанных с белками реакционного центра фотосистемы 2 (ФС-2); Z - вторичный донор электрона ФС-2, (остаток тирозина); Пбао - первичный донор электрона ФС-2 (димер хлорофилла); *П680 - возбужденное состояние хлорофилла П680; Фео - первичный акцептор электрона ФС-2, феофитин; QA и QB -акцепторы электрона хиноновой природы; цит в./f-комплекс цитохромов, участвующих в переносе электрона от ФС-2 к фотосистеме 1 (ФС-1); Пц - пластоцианин (подвижный переносчик электрона); П700 - первичный донор электрона ФС-1 (димер хлорофилла); *П700 - возбужденное состояние П700;Хла-(хлорофилл) и Ох-(хинон), соответственно, первичный и вторичный акцепторы электрона ФС-1; Fx, Fa и Fb акцепторы электрона ФС-1 (Fe-S-центры); Фд - ферредоксинрастворимый переносчик электрона (Fe-S-содержащий белок); НАДФ+ - никотинамидаденин динуклеотид фосфат (конечный переносчик электронов, используемый вместе с АТФ в ассимиляции СО2), hv - квант света. По вертикальной шкале указаны приблизительные значения окислительно-восстановительных потенциалов переносчиков электрона при рН 7.
раций ионов Н+ по обе стороны тилакоидной мембраны, которая, как и в случае митохондрий, необходима для осуществления процесса фосфо-рилирования — образования АТФ, основного энергетического эквивалента, используемого в качестве источника энергии в биологических процессах. Образованные в результате фотохимического переноса электронов АТФ и НАДФН используются для восстановления СО2 с образованием первичных са-харов, которое в упрощенном виде можно описать следующим образом: СО2 + 4е + 4Н+ —*• СН2О + + Н2О. При этом на каждую молекулу СО2 расходуется две молекулы НАДФН и три молекулы АТФ. Этот процесс, в результате которого "восстановленная" молекула СО2 включается в состав гексозы, осуществляется через ряд стадий с участием сложного цикла энзиматических реакций, получившего название цикла Кальвина по имени его открывателя. В заключение необходимо отметить, что исследование фотосинтеза — сложнейшего фундаментального биологического процесса, имеющее давние традиции в отечественной науке, привлекает в настоящее время внимание все большего числа естествоиспытателей — биологов, физиков, химиков, математиков. Познание молекулярных механизмов фотосинтеза будет иметь большое значение для обеспечения человечества экологически чистой энергией за счет практически неиссякаемого источника — солнечного излучения (например, на основе фоторазложения воды на молекулярной водород и кислород), для повышения фотосинтетической продуктивности растений, лежащей в основе обеспечения человечества пищей, для использования принципов фотопреобразования световой энергии при фотосинтезе в фотобиотехнологических и фотобиотехнических системах, для обеспечения длительных космических экспедиций органикой и молекулярным кислородом, для решения проблем экологической безопасности отдельных регионов, для сохранения и развития биосферы.
ЗАКЛЮЧЕНИЕ
Знания, накопленные при изучении современных организмов различной степени сложности, позволяют сформулировать непротиворечивую концепцию эволюции биоэнергетических систем. Эта концепция дает ключ к пониманию не только путей становления механизмов превращения энергии в клетке, но и позволяет объяснить, почему химия и физика живой клетки базируются на двух основных классах веществ: а) нуклеиновых кислотах и нуклео-тидах и б) белках. Вкратце система взглядов, о которой идет речь, может быть суммирована следующей схемой эволюции жизни.
1. Образование азотистых оснований (пуринов и пиримидинов), а затем и нуклеотидов из Н2О, NH3, СО2, HCN и некоторых других простейших соединений под действием ультрафиолетового излучения Солнца.
2. Использование остатков аденина, а затем также других пуринов и пиримидинов в нуклеотидах для поглощения ультрафиолетового света. При
этом энергия ультрафиолетовых квантов оказывается движущей силой для синтеза АТФ из АДФ и фосфата или для осуществления других энергоемких реакций коферментами-нуклеотидами (адени-новый фотосинтез).
3. Образование резервных веществ за счет энергии АТФ (гликогенез) с тем, чтобы их последующее расщепление могло поддержать ресинтез АТФ при отсутствии ультрафиолетового света (гликолиз).
4. Изменение спектральных свойств атмосферы, ставшей плохо проницаемой для ультрафиолета, и замена "аденинового" фотосинтеза на фотосинтез, использующий видимый свет. В качестве пигментов используется ретиналь, а затем хлорофилл. В результате АТФ, бывший до того как преобразователем световой энергии, так и "конвертируемой энергетической валютой", утрачивает первую из этих двух функций, сохранив только вторую.
5. Увеличение концентрации О2 в атмосфере в результате деятельности фотосинтезирующих организмов и появление ферментов, поглощающих кислород с целью его детоксикации.
6. Создание современных дыхательных систем, преобразующих в АТФ энергию окисления субстратов кислородом.
СПИСОК ЛИТЕРАТУРЫ:
1. Будыко М.И., РоновА.Б., Яншин А.Л. История атмосферы. Л.: Гидрометеоиздат, 1985.
2. Мак-Ивен М., Филяипс Л. Химия атмосферы. М.: Мир, 1978.
3. Фотосинтез / Под ред. Говинжи. М.: Мир. Т. 1 и 2. 1987.
4. Холя Д., Рао К. Фотосинтез. М.: Мир, 1983.
5. Клейтон Р. Фотосинтез. Физические механизмы и химические модели. М.: Мир, 1984.
6. Шувалов В.А. Первичное преобразование световой энергии при фотосинтезе. М.: Наука, 1990.
7. Уайт А., Хендяер Ф.. Смит Р. и др. Основы биохимии. М.: Мир, 1981.
8. Саган К. В. V Происхождение предбиологических систем/Подрех А.И. Опарина. М.: Мир, 1966. С. 211.
9. Понамперума С.В. // Там же. С. 224.
10. Ску.шчев В.П. Аккумуляция энергии в клетке. М.: Наука, 1969.
11. Скулачев В.П. Мембранные преобразователи энергии. М.: Высш. шк., 1989.
12. Ску.ючев В.П. Энергетика биологических мембран. М.: Наука, 1989.
13. Скулачев В.П. Кислород в живой клетке: добро и зло // Соросовский Образовательный Журнал. 1996. № 3. С. 4-16.
14. Скулачев В.П. Законы биоэнергетики //Там же. 1997. № 1. С. 9-14.


